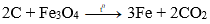Hóa học 9 Bài 32: Luyện tập chương 3: Phi kim – Sơ lược về bảng tuần hoàn các nguyên tố hóa học được biên soạn hy vọng sẽ là là tài liệu hữu ích giúp các em nắm vững kiến thức bài học và đạt kết quả tốt trong các bài thi, bài kiểm tra trên lớp.
Tóm tắt lý thuyết Hóa học 9 Bài 32
1. Tính chất hóa học của phi kim
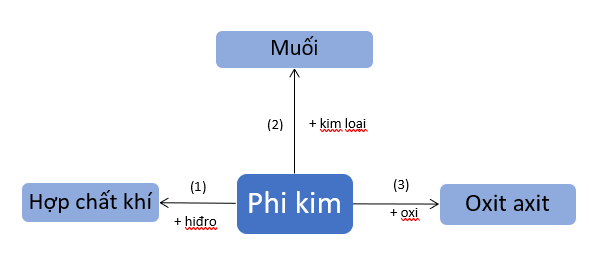
2. Tính chất hóa học của 1 số phi kim cụ thể
a) Tính chất hóa học của clo

b) Tính chất hóa học các hợp chất của cacbon

3. Bảng tuần hoàn các nguyên tố hóa học
a) Cấu tạo của bảng tuần hoàn
– Ô nguyên tố
– Chu kỳ
– Nhóm
b) Sự biến đổi tính chất của các nguyên tố trong bảng tuần hoàn
– Trong một chu kỳ, khi đi từ đầu đến cuối chu kỳ theo chiều tăng của điện tích hạt nhân:
+) Số electron lớp ngoài cùng của nguyên tử tăng dần từ 1 đến 8 electron.
+) Tính kim loại của các nguyên tố giảm dần, đồng thời tính phi kim của các nguyên tố tăng dần.
– Trong một nhóm, khi đi từ trên xuống dưới theo chiều tăng của điện tích hạt nhân:
+) Số lớp electron của nguyên tử tăng dần.
+) Tính kim loại của các nguyên tố tăng dần, đồng thời tính phi kim của các nguyên tố giảm dần.
c) Ý nghĩa bảng tuần hoàn
Biết vị trí của nguyên tố trong bảng tuần hoàn ta có thể suy đoán cấu tạo nguyên tử và ngược lại.

Giải bài tập SGK Hóa học 9 Bài 32
Bài 1 (trang 103 SGK Hóa 9)
Căn cứ vào sơ đồ sau:

Hãy viết phương trình hóa học với phi kim cụ thể là lưu huỳnh.
Lời giải:

Bài 2 (trang 103 SGK Hóa 9)
Hãy viết các phương trình hóa học biểu diễn tính chất hóa học của clo theo sơ đồ sau:

Lời giải:

Bài 3 (trang 103 SGK Hóa 9)
Hãy viết các phương trình hóa học biểu diễn tính chất hóa học của cacbon và một số hợp chất của nó theo sơ đồ 3. Cho biết vai trò của cacbon trong phản ứng đó.

Lời giải:
PTHH biểu diễn tính chất hóa học của cacbon và một số hợp chất khác:
(1) C(r) + CO2 (k) ![]() 2CO(k)
2CO(k)
(2) C(r) + O2 (k) ![]() CO2
CO2
(3) CO + CuO ![]() Cur + CO2 (k)
Cur + CO2 (k)
(4) CO2 (k) + C(r) ![]() 2CO(k)
2CO(k)
(5) CO2 (k) + CaO(r) ![]() CaCO3 (r)
CaCO3 (r)
(6) CO2(k) + 2NaOH(dd) dư → Na2CO3 (r) + H2O(l)
CO2 (k) + NaOH (dd) đủ → NaHCO3
(7) CaCO3 (r) ![]() CaO(r) + CO2 (k)
CaO(r) + CO2 (k)
(8) Na2CO3(r) + 2HCl(dd) → 2NaCl(dd) + CO2(k)↑ + H2O(l)
NaHCO3 (r) + HCl (dd) → NaCl(dd) + CO2(k) + H2O(l)
Vai trò của C trong phản ứng (1), (2) và (4) là chất khử (chất chiếm oxi).
Bài 4 (trang 103 SGK Hóa 9)
Nguyên tố A có số hiệu nguyên tử là 11, chu kì 3, nhóm I trong bảng hệ thống tuần hoàn. Hãy cho biết:
– Cấu tạo nguyên tử của A.
– Tính chất hóa học đặc trưng của A.
– So sánh tính chất hóa học của A với các nguyên tố lân cận.
Lời giải:
a) Cấu tạo nguyên tử của A:
Số hiệu nguyên tử của A là 11 cho biết: natri ở ô số 11, điện tích hạt nhân nguyên tử natri là 11+ có 11 electron trong nguyên tử natri, ở chu kì 3, nhóm I.
b) Tính chất hóa học đặc trưng của natri:
Nguyên tố natri ở đầu chu kì là hai kim loại mạnh, tròn phản ứng hóa học, natri là chất khử mạnh.
Tác dụng với phi kim:
4Na + O2 → 2Na2O
2Na + Cl2 → 2NaCl
Tác dụng với dung dịch axit:
2Na + 2HCl → 2NaCl + H2 ↑
Tác dụng với nước: Nguyên tố Na ngoài tính chất hóa học chung của kim loại còn có tính chất hóa học đặc trưng là tác dụng với H2O ở nhiệt độ thường.
2Na + 2H2O → 2NaOH + H2 ↑
Tác dụng với dung dịch muối: Na + dung dịch CuSO4
2Na + 2H2O → 2NaOH +H2 ↑
2NaOH + CuSO4 → Cu(OH)2 ↓ +Na2SO4
c) So sánh tính chất hóa học của Na với các nguyên tố lân cận:
Na có tính chất hóa hoc mạnh hơn Mg (nguyên tố sau Na), mạnh hơn Li (nguyên tố trên Na) nhưng yếu hơn K (nguyên tố dưới Na).
Bài 5 (trang 103 SGK Hóa 9)
a) Hãy xác định công thức của một loại oxit sắt, biết rằng khi cho 32g oxit sắt này tác dụng hoàn toàn với khí cacbon oxit thì thu được 22,4g chất rắn.
Biết khối lượng mol của oxit sắt là 160 gam.
b) Chất khí sinh ra được hấp thụ hoàn toàn trong dung dịch nước vôi trong có dư. Tính khối lượng kết tủa thu được.
Lời giải:
a) Gọi công thức của oxit sắt là: FexOy
PTHH:


Do đó x : y = 2 : 3.
Vậy CTHH của oxit sắt: Fe2O3.
b) Khí sinh ra CO2
PTHH:

Theo pt (1) : ![]()
Theo pt (2) ⇒ nCaCO3 = nCO2 = 0,6 (mol)
mCaCO3 = 0,6.100 = 60 (g).
Bài 6 (trang 103 SGK Hóa 9)
Cho 69,6g MnO2 tác dụng với dung dịch HCl đặc dư thu được một lượng khí X. Dẫn khí X vào 500ml dung dịch NaOH 4M thu được dung dịch A. Tính nồng độ mol của các chất trong dung dịch A. Giả thiết rằng thể tích dung dịch sau phản ứng thay đổi không đáng kể.
Lời giải:
![]()
VNaOH = 500ml = 0,5 lít ⇒ nNaOH = CM. V= 0,5 x 4 = 2 mol.
Phương trình phản ứng:
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O.
Theo pt: nCl2 = nMnO2 = 0,8 mol.
Cl2 + 2NaOH → NaCl + NaClO + H2O.
Ta có tỉ lệ:  → NaOH dư nên tính nNaCl và nNaClO theo nCl2
→ NaOH dư nên tính nNaCl và nNaClO theo nCl2
Theo pt: nNaCl = nNaClO = nCl2 = 0,8 mol.
CM(NaCl)= CM(NaClO) = = 1,6 mol/l.
Theo pt: nNaOH pư = 2. nCl2 = 2. 0,8 = 1,6mol.
CM(NaOH) dư = ![]() = 0,8 mol/l.
= 0,8 mol/l.
Trắc nghiệm Hóa học 9 Bài 32 (có đáp án)
Câu 1: Nguyên tố X có hiệu số nguyên tử là 9. Điều khẳng định nào sau đây không đúng ?
A. Điện tích hạt nhân của nguyên tử là 9+, nguyên tử có 9 electron.
B. Nguyên tử X ở gần cuối chu kỳ 2, đầu nhóm VII.
C. X là 1 phi kim hoạt động mạnh.
D. X là 1 kim loại hoạt động yếu.
Đáp án: D
Câu 2: Cặp chất tác dụng được với dung dịch KOH là
A. CO, SO2
B. SO2, SO3
C. FeO, Fe2O3
D. NO, NO2
Đáp án: B
SO2 và SO3 là các oxit axit nên tác dụng được với dung dịch KOH
Phương trình hóa học:
SO2 + 2KOH → K2SO3 + H2O
SO3 + 2KOH → K2SO4 + H2O
Câu 3: Chất khí nào sau đây có thể gây chết người vì ngăn cản sự vận chuyển oxi trong máu ?
A. CO
B. CO2
C. SO2
D. NO
Đáp án: A
Câu 4: Khi dẫn khí clo vào cốc đựng nước, sau đó cho vào cốc 1 mẩu quỳ tím. Hiện tượng xảy ra là
A. quỳ tím hóa đỏ.
B. quỳ tím hóa xanh.
C. quỳ tím không chuyển màu.
D. quỳ tím hóa đỏ sau đó mất màu ngay.
Đáp án: D
Câu 5: Phản ứng giữa Cl2 và dung dịch NaOH ở điều kiện thường dùng để điều chế
A. thuốc tím.
B. nước gia – ven.
C. clorua vôi.
D. kali clorat.
Đáp án: B
Câu 6: Trong thực tế, người ta có thể dùng cacbon để khử oxit kim loại nào trong số các oxit kim loại dưới đây để sản xuất kim loại ?
A. Al2O3
B. K2O
C. CaO
D. Fe3O4
Đáp án: D
Cacbon khử được oxit của những kim loại đứng sau nhôm trong dãy hoạt động hóa học
Câu 7: Trong các chất sau chất nào có thể tham gia phản ứng với clo ?
A. Oxi.
B. Dung dịch KOH.
C. CuO.
D. NaCl.
Đáp án: B
Cl2 + 2KOH → KCl + KClO + H2O
Câu 8: Khí CO lẫn tạp chất là CO2 và SO2 có thể làm sạch CO bằng cách dẫn mẫu khí trên qua
A. dung dịch H2SO4 đặc.
B. dung dịch Ca(OH)2.
C. dung dịch CaSO4.
D. dung dịch CaCl2.
Đáp án: B
Dẫn hỗn hợp khí qua dung dịch Ca(OH)2 dư. Khí SO2 và CO2 phản ứng bị giữ lại, khí CO không phản ứng thoát ra khỏi dung dịch thu được CO tinh khiết.
SO2 + Ca(OH)2 → CaSO3 ↓ + H2O
CO2 + Ca(OH)2 → CaCO3 ↓ + H2O
Câu 9: Đốt cháy hoàn toàn 3 gam C thành CO2. Cho toàn bộ sản phẩm hấp thụ vào dung dịch nước vôi trong dư. Khối lượng kết tủa tạo thành là
A. 50 gam.
B. 25 gam.
C. 15 gam.
D. 40 gam.
Đáp án: B
Ta có: nC = 3 : 12 = 0,25 mol

Khối lượng kết tủa: m = 0,25.100 = 25 gam.
Câu 10: Cho 69,6 gam MnO2 tác dụng với dung dịch HCl đặc, nóng, dư. Thể tích khí ở điều kiện tiêu chuẩn thu được là
A. 4,48 lít.
B. 6,72 lít.
C. 17,92 lít.
D. 13,44 lít.
Đáp án: C

Câu 11: Thể tích của dung dịch KOH 1M ở điều kiện thường cần dùng để tác dụng hoàn toàn với 1,12 lít khí Cl2 (đktc) là
A. 0,2 lít.
B. 0,3 lít.
C. 0,4 lít.
D. 0,1 lít.
Đáp án: D

Câu 12: Một nguyên tố X ở ô thứ 12 trong bảng tuần hoàn. Điện tích hạt nhân nguyên tử X là
A. 12-.
B. 12+.
C. -12.
D. +12.
Đáp án: B
Câu 13: Số thứ tự ô nguyên tố trong bảng hệ thống tuần hoàn bằng:
A. số hiệu nguyên tử
B. nguyên tử khối
C. số nơtron
D. số lớp electron.
Đáp án: A.
Câu 14: Trong bảng hệ thống tuần hoàn các nguyên tố hóa học, số chu kì nhỏ và chu kì lớn lần lượt là
A. 3 và 3
B. 4 và 3
C. 3 và 4
D. 4 và 4
Đáp án: C
Câu 15: Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân
A. tính kim loại tăng dần.
B. tính phi kim tăng dần.
C. tính kim loại không đổi.
D. tính phi kim giảm dần.
Đáp án: B
******************
Trên đây là nội dung bài học Hóa học 9 Bài 32: Luyện tập chương 3: Phi kim – Sơ lược về bảng tuần hoàn các nguyên tố hóa học do biên soạn bao gồm phần lý thuyết, giải bài tập và các câu hỏi trắc nghiệm có đáp án đầy đủ. Hy vọng các em sẽ nắm vững kiến thức về Luyện tập chương 3: Phi kim – Sơ lược về bảng tuần hoàn các nguyên tố hóa học. Chúc các em học tập thật tốt và luôn đạt điểm cao trong các bài thi bài kiểm tra trên lớp.
Biên soạn bởi: Trường
Đăng bởi: Thcs-thptlongphu.edu.vn
Chuyên mục: Tổng hợp