Hóa học 9 Bài 31: Sơ lược về bảng tuần hoàn các nguyên tố hóa học được biên soạn hy vọng sẽ là là tài liệu hữu ích giúp các em nắm vững kiến thức bài học và đạt kết quả tốt trong các bài thi, bài kiểm tra trên lớp.
Tóm tắt lý thuyết Hóa học 9 Bài 31
I. NGUYÊN TẮC SẮP XẾP CÁC NGUYÊN TỐ TRONG BẢNG TUẦN HOÀN
Các nguyên tố trong bảng tuần hoàn được sắp xếp theo chiều tăng dần của điện tích hạt nhân nguyên tử.
II. CẤU TẠO BẢNG TUẦN HOÀN
1. Ô nguyên tố
– Ô nguyên tố cho biết: Số hiệu nguyên tử, kí hiệu hóa học, tên nguyên tố, nguyên tử khối của nguyên tố đó.
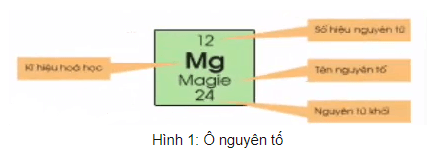
– Số hiệu nguyên tử có số trị bằng số đơn vị điện tích hạt nhân và bằng số electron trong nguyên tử. Số hiệu nguyên tử trùng với số thứ tự ô trong bảng tuần hoàn.
Ví dụ:
Số hiệu nguyên tử của nhôm là 13 cho biết: nhôm ở ô thứ 13 trong bảng tuần hoàn, điện tích hạt nhân nguyên tử nhôm là 13+ (hay số đơn vị điện tích hạt nhân là 13), có 13 electron trong nguyên tử nhôm.
2. Chu kì
– Chu kỳ là dãy các nguyên tố mà nguyên tử của chúng có cùng số lớp electron và được xếp theo chiều điện tích hạt nhân tăng dần.
– Số thứ tự chu kì bằng số lớp electron.
– Bảng tuần hoàn gồm có 7 chu kỳ: chu kỳ 1, 2, 3 là các chu kỳ nhỏ. Chu kỳ 4, 5, 6, 7 là các chu kỳ lớn. Ví dụ
+) Chu kì 2: Gồm 8 nguyên tố từ Li đến Ne, có 2 lớp electron trong nguyên tử. Điện tích hạt nhân tăng dần từ Li là 3+,… đến Ne là 10+.
+) Mô phỏng cấu tạo nguyên tử O ở chu kỳ 2, có 2 lớp electron.

3. Nhóm
– Nhóm gồm các nguyên tố mà nguyên tử của chúng có số electron lớp ngoài cùng bằng nhau, do đó có tính chất tương tự nhau được xếp thành một cột theo chiều tăng của điện tích hạt nhân nguyên tử.
– Số thứ tự của các nhóm A bằng số electron ở lớp ngoài cùng của nguyên tử trong nhóm đó.
Ví dụ:
+) Nhóm IA: Gồm các nguyên tố kim loại hoạt động mạnh. Nguyên tử của chúng đều có 1 electron ở lớp ngoài cùng. Điện tích hạt nhân tăng từ Li (3+), … đến Fr (87+).
+) Mô phỏng cấu tạo nguyên tử Kali ở nhóm IA, có 1 electron ở lớp ngoài cùng:

III. SỰ BIỂN ĐỔI TÍNH CHẤT CỦA CÁC NGUYÊN TỐ TRONG BẢNG TUẦN HOÀN
1. Trong một chu kì
Trong một chu kỳ, khi đi từ đầu đến cuối chu kỳ theo chiều tăng của điện tích hạt nhân:
– Số e lớp ngoài cùng của nguyên tử tăng dần từ 1 đến 8 electron.
– Tính kim loại của các nguyên tố giảm dần, đồng thời tính phi kim của các nguyên tố tăng dần.
Ví dụ:
Chu kì 2 gồm 8 nguyên tố:

+ Số e lớp ngoài cùng của nguyên tử các nguyên tố trong chu kỳ 2 tăng dần từ 1 đến 8
+ Đẩu chu kỳ 2 là một kim loại mạnh (Li), cuối chu kỳ là một phi kim mạnh (F), kết thúc chu kỳ là một khí hiếm (Ne).
2. Trong một nhóm
Trong một nhóm, khi đi từ trên xuống dưới theo chiều tăng của điện tích hạt nhân.
– Số lớp electron của nguyên tử tăng dần.
– Tính kim loại của các nguyên tố tăng dần, đồng thời tính phi kim của các nguyên tố giảm dần.
Ví dụ:
Nhóm IA gồm 6 nguyên tố từ Li đến Fr
+) Số lớp electron tăng dần từ 2 đến 7. Số electron lớp ngoài cùng của nguyên tử đều bằng 1.
+) Tính kim loại của các nguyên tố tăng dần. Đầu nhóm IA, Li là kim loại hoạt động hóa học mạnh cuối nhóm là kim loại Fr hoạt động hóa học rất mạnh
IV. Ý NGHĨA CỦA BẢNG TUẦN HOÀN CÁC NGUYÊN TỐ HÓA HỌC
1. Biết vị trí của nguyên tố ta có thể suy đoán cấu tạo nguyên tử và tính chất của nguyên tố.
Ví dụ:
Biết: Nguyên tố A có số hiệu nguyên tử là 17, chu kì 3, nhóm VIIA.
Xác định được:
+) Nguyên tố A có số hiệu nguyên tử là 17, suy ra điện tích hạt nhân của nguyên tử A là 17+, nguyên tử A có 17 electron.
+) A ở chu kì 3, suy ra nguyên tử A có 3 lớp electron. Vì ở gần cuối chu kì 3 nên A là một phi kim mạnh, tính phi kim của A mạnh hơn của nguyên tố trước nó trong cùng chu kì (là S có số hiệu là 16).
+) A ở nhóm VIIA nên lớp ngoài cùng có 7 electron, tính phi kim của A yếu hơn của nguyên tố phía trên nó trong cùng nhóm (là F có số hiệu nguyên tử là 9) nhưng mạnh hơn nguyên tố đứng dưới nó trong cùng nhóm (là Br có số hiệu nguyên tử là 35).
2. Biết cấu tạo nguyên tử của nguyên tố có thể suy đoán vị trí và tính chất nguyên tố đó.
Ví dụ:
Biết: Nguyên tố X có điện tích hạt nhân là 11+, nguyên tử X có 3 lớp electron, lớp ngoài cùng có 1 electron.
Xác định được:
+ Nguyên tử X có điện tích hạt nhân là 11+ suy ra X ở ô 11
+ Nguyên tử X có 3 lớp electron nên X ở chu kỳ 3
+ Nguyên tử X có 1e ở lớp ngoài cùng nên X ở nhóm IA.
– Nguyên tố X là kim loại vì ở đầu chu kì
Giải bài tập SGK Hóa học 9 Bài 31
Bài 1 (trang 101 SGK Hóa 9)
Dựa vào bảng tuần hoàn, hãy cho biết cấu tạo nguyên tử, tính chất kim loại, phi kim của các nguyên tố có số hiệu nguyên tử 7, 12, 16.
Lời giải:
| Số hiệu nguyên tử | Cấu tạo nguyên tử | Tính chất | ||||
| Điện tích hạt nhân | Số e trong nguyên tử | Số lớp electron | Số e lớp ngoài cùng | Kim loại | Phi kim | |
| 7 | 7+ | 7 | 2 | 5 | x | |
| 12 | 12+ | 12 | 3 | 2 | x | |
| 16 | 6+ | 6 | 3 | 6 | x | |
+ Giả sử nguyên tố A có số hiệu nguyên tử là 7 ⇒ A thuộc ô số 7 trong bảng tuần hoàn, có điện tích hạt nhân là 7+, có 7eletron
Dựa vào bảng tuần hoàn ta thấy nguyên tố A thuộc chu kì 2 ⇒ có 2 lớp eletron; thuộc nhóm V ⇒ có 5 eletron lớp ngoài cùng và phi kim.
+ Tương tự với 2 nguyên tố còn lại ta được kết quả trong bảng.
Bài 2 (trang 101 SGK Hóa 9)
Biết X có cấu tạo nguyên tử như sau : điện tích hạt nhân là 11+, 3 lớp electron, lớp ngoài cùng có 1 electron. Hãy suy ra vị trí của X trong bảng tuần hoàn và tính chất hoá học cơ bản của nó.
Lời giải:
Điện tích hạt nhân là 11+ nên số thứ tự của nguyên tố là 11 ( ô số 11)
Có 3 lớp e ⇒ thuộc chu kì 3,
Có 1 e lớp ngoài cùng ⇒ thuộc nhóm I trong bảng tuần hoàn
Tên nguyên tố là: Natri.
Kí hiệu hóa học: Na.
Nguyên tử khối: 23.
Bài 3 (trang 101 SGK Hóa 9)
Các nguyên tố trong nhóm I đều là những kim loại mạnh tương tự natri: tác dụng với nước tạo thành dung dịch kiềm giải phóng hiđro, tác dụng với oxi tạo thành oxit, tác dụng với phi kim khác tạo thành muối … Viết các phương trình hóa học minh họa với kali.
Lời giải:
Phương trình hóa học:
– Tác dụng với nước tạo dung dịch kiềm và giải phóng khí H2
2K + 2H2O → 2KOH + H2
– Tác dụng với oxi tạo thành oxit
4K + O2 → 2K2O
-Tác dụng với phi kim tạo thành muối
2K + Cl2 → 2KCl.
Bài 4 (trang 101 SGK Hóa 9)
Các nguyên tố nhóm VII đều là những phi kim mạnh tương tự clo (trừ At), tác dụng với hầu hết kim loại tạo muối, tác dụng với hiđro tạo hợp chất khí. Viết phương trình hóa học minh họa với brom.
Lời giải:
Phương trình hóa học:
Br2 + 2K ![]() 2KBr
2KBr
Br2 + H2 ![]() 2HBr
2HBr
Br2 + Cu ![]() CuBr2
CuBr2
Bài 5 (trang 101 SGK Hóa 9)
Hãy cho biết các sắp xếp nào sau đây đúng theo chiều tính kim loại giảm dần:
a) Na, Mg, Al, K.
b) K, Na, Mg, Al.
c) Al, K, Na, Mg.
d) Mg, K, Al, Na.
Giải thích sự lựa chọn.
Lời giải:
Chọn đáp án b).
Giải thích:
– K cùng nhóm với Na: trong cùng 1 nhóm theo chiều tăng dần điện tích hạt nhân tính kim loại tăng dần ⇒ Tính kim loại của Na < K
– Na, Mg, Al cùng chu kì: trong cùng 1 chu kì theo chiều tăng dần điện tích hạt nhân tính kim loại giảm dần ⇒ Tính kim loại Na > Mg > Al
⇒ Dãy sắp xếp chiều tính kim loại giảm dần là K > Na > Mg > Al ⇒ Đáp án B
Bài 6 (trang 101 SGK Hóa 9)
Hãy sắp xếp các nguyên tố sau theo chiều tính phi kim tăng dần: F, O, N, P, As. Giải thích.
Lời giải:
Các nguyên tố theo chiều tăng dần của phi kim: As, P, N, O, F.
Giải thích:
– As, P, N cùng ở nhóm V theo quy luật biến thiên tính chất trong nhóm ta biết trong cùng 1 nhóm theo chiều tăng dần điện tích hạt nhân tính phi kim giảm dần
⇒ Tính phi kim N > P > As
– N, O, F cùng thuộc chu kì 2 theo quy luật biến thiên tính chất ta biết trong cùng 1 chu kì theo chiều tăng dần điện tích hạt nhân tính phi kim tăng dần
⇒ Tính phi kim N < O < F
⇒Dãy sắp xếp các nguyên tố theo chiều tính phi kim tăng dần là: As < P < N < O < F
Bài 7 (trang 101 SGK Hóa 9)
a) Hãy xác định công thức của hợp chất khí A, biết rằng:
– A là oxit của lưu huỳnh chứa 50% oxi.
– 1 gam khí A chiếm 0,35 lít ở đktc.
b) Hòa tan 12,8g hợp chất khí A vào 300ml dung dịch NaOH 1,2M. Hãy cho biết muối nào thu được sau phản ứng? Tính nồng độ của muối (giả thiết thể tích dung dịch thay đổi không đáng kể).
Lời giải:

Đặt công thức phân tử của A là SxOy.
Lập tỉ số về khối lượng để tính các chỉ số x và y.

Công thức phân tử của A là SO2.

VNaOH = 300ml = 0,3 l;
nNaOH = CM. V = 1,2 x 0,3 = 0,36 mol.
Xét xem có tạo hai muối không?
So sánh tỉ lệ mol của SO2 : NaOH = 0,2 : 0,36 = 1,1 : 1,8
Như vậy khi cho SO2 vào dung dịch NaOH có các phản ứng:
SO2 + NaOH → NaHSO3.
SO2 + 2NaOH → Na2SO3 + H2O.
Gọi nNaHSO3 = x, nNa2SO3 = y.
nSO2 = x + y = 0,2 mol.
nNaOH = x + 2y = 0,36 mol.
Giải hệ phương trình ta có: x = 0,04 mol; y = 0,16 mol.

Trắc nghiệm Hóa học 9 Bài 31 (có đáp án)
Câu 1: Nhóm các nguyên tố được sắp xếp theo chiều tính phi kim tăng dần là
A. O, F, N, C.
B. F, O, N, C.
C. O, N, C, F.
D. C, N, O, F.
Đáp án: D
Các nguyên tố C, N, O, F cùng thuộc chu kỳ 2;
Trong một chu kỳ, theo chiều tăng của điện tích hạt nhân tính phi kim của các nguyên tố tăng dần
→ Tính phi kim: C < N < O < F.
Câu 2: Trong 1 chu kỳ (trừ chu kì 1), đi từ trái sang phải tính chất của các nguyên tố biến đổi như sau
A. tính kim loại và tính phi kim đều giảm dần.
B. tính kim loại và tính phi kim đều tăng dần.
C. tính kim loại giảm dần đồng thời tính phi kim tăng dần.
D. tính kim loại tăng dần đồng thời tính phi kim giảm dần.
Đáp án: C
Câu 3: Dãy các kim loại nào sau đây được sắp xếp theo chiều tính kim loại tăng dần ?
A. K, Na, Li, Rb.
B. Li, K, Rb, Na.
C. Na, Li, Rb, K.
D. Li, Na, K, Rb.
Đáp án: D
Các kim loại Li, Na, K, Rb thuộc cùng nhóm IA trong bảng tuần hoàn.
Trong cùng một nhóm, theo chiều tăng của điện tích hạt nhân tính kim loại của các nguyên tố tăng dần
→ Tính kim loại: Li < Na < K < Rb.
Câu 4: Cho các nguyên tố sau O, P, N. Hãy chỉ ra thứ tự sắp xếp đúng theo chiều tính phi kim tăng dần
A. O, P, N.
B. N, P, O.
C. P, N, O.
D. O, N, P.
Đáp án: C
Ta có: P và N cùng thuộc nhóm VA, theo quy luật biến đổi xác định được tính phi kim của P < N.
O và N cùng thuộc chu kỳ 2, theo quy luật biến đổi xác định được tính phi kim của N < O.
Chiều tăng dần tính phi kim là: P < N < O.
Câu 5: Biết X có cấu tạo nguyên tử như sau: điện tích hạt nhân là 12+, có 3 lớp electron, lớp ngoài cùng có 2 electron. Vị trí của X trong bảng tuần hoàn là
A. chu kỳ 3, nhóm II.
B. chu kỳ 3, nhóm III.
C. chu kỳ 2, nhóm II.
D. chu kỳ 2, nhóm III.
Đáp án: A
X có 3 lớp electron → X thuộc chu kỳ 3
Lớp ngoài cùng của X có 2 electron → X thuộc nhóm II.
Câu 6: Nguyên tử của nguyên tố X có 3 lớp electron, lớp electron ngoài cùng có 7 electron. Vị trí và tính chất cơ bản của nguyên tố X là
A. thuộc chu kỳ 3, nhóm VII là kim loại mạnh.
B. thuộc chu kỳ 7, nhóm III là kim loại yếu.
C. thuộc chu kỳ 3, nhóm VII là phi kim mạnh.
D. thuộc chu kỳ 3, nhóm VII là phi kim yếu.
Đáp án: C
X có 3 lớp electron → X thuộc chu kỳ 3
Lớp ngoài cùng của X có 7 electron → X thuộc nhóm VII.
X ở phía cuối chu kỳ nên là phi kim mạnh.
Câu 7: Trong chu kỳ 3, X là nguyên tố đứng đầu chu kỳ, còn Y là nguyên tố đứng cuối chu kỳ nhưng trước khí hiếm. Nguyên tố X và Y có tính chất sau
A. X là kim loại mạnh, Y là phi kim yếu.
B. X là kim loại mạnh, Y là phi kim mạnh.
C. X là kim loại yếu, Y là phi kim mạnh.
D. X là kim loại yếu, Y là phi kim yếu.
Đáp án: B
Câu 8: Nguyên tố M có số hiệu nguyên tử là 19, chu kỳ 4, nhóm I trong bảng tuần hoàn các nguyên tố hóa học. Phát biểu nào sau đây đúng ?
A. Điện tích hạt nhân 19+, 4 lớp electron, lớp ngoài cùng có 1 electron, kim loại mạnh.
B. Điện tích hạt nhân 19+, 1 lớp electron, lớp ngoài cùng có 4 electron, kim loại mạnh.
C. Điện tích hạt nhân 19+, 4 lớp electron, lớp ngoài cùng có 4 electron, kim loại yếu.
D. Điện tích hạt nhân 19+, 4 lớp electron, lớp ngoài cùng có 1 electron, kim loại yếu.
Đáp án: A
M có số hiệu nguyên tử là 19 nên điện tích hạt nhân nguyên tử M là 19+.
M thuộc chu kỳ 4 nên có 4 lớp electron trong nguyên tử; M thuộc nhóm I nên lớp ngoài cùng có 1 electron.
M đứng ở đầu chu kỳ nên là kim loại mạnh.
Câu 9: Nguyên tố X ở chu kỳ 4 nhóm VI, nguyên tố Y ở chu kỳ 2 nhóm VII. So sánh tính chất của X và Y thấy
A. tính phi kim của X mạnh hơn Y.
B. tính phi kim của Y mạnh hơn X.
C. X, Y có tính phi kim tương đương nhau.
D. X, Y có tính kim loại tương đương nhau.
Đáp án: B
Theo quy luật biến đổi tính chất các nguyên tố trong bảng tuần hoàn xác định được Y là phi kim mạnh nhất. Do đó, tính phi kim của Y mạnh hơn X.
Câu 10: Nguyên tố X có hiệu số nguyên tử là 10. Điều khẳng định nào sau đây không đúng ?
A. Điện tích hạt nhân của nguyên tử là 10+, nguyên tử có 10 electron.
B. Nguyên tử X cuối chu kỳ 2.
C. X là một khí hiếm.
D. X là 1 kim loại hoạt động yếu.
Đáp án: D
******************
Trên đây là nội dung bài học Hóa học 9 Bài 31: Sơ lược về bảng tuần hoàn các nguyên tố hóa học do biên soạn bao gồm phần lý thuyết, giải bài tập và các câu hỏi trắc nghiệm có đáp án đầy đủ. Hy vọng các em sẽ nắm vững kiến thức về Sơ lược về bảng tuần hoàn các nguyên tố hóa học. Chúc các em học tập thật tốt và luôn đạt điểm cao trong các bài thi bài kiểm tra trên lớp.
Biên soạn bởi: Trường
Đăng bởi: Thcs-thptlongphu.edu.vn
Chuyên mục: Tổng hợp